Đề bài: A. x <y <z B. y<z< x C. z<x <y D. z<y <x ĐÁP ÁN: C Academia.edu no longer supports Internet Explorer. To browse Academia.edu and the wider internet faster and more securely, please take a few seconds to upgrade your browser.
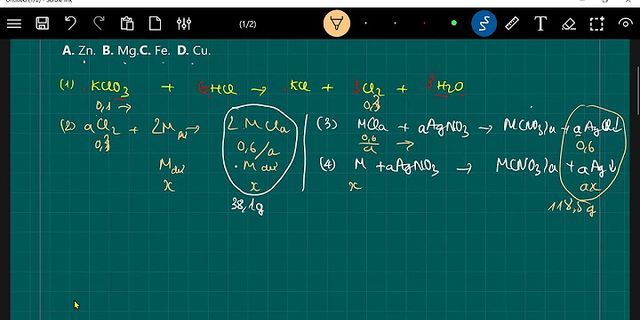
a. pH = 1 —> [H+] = 0,1 —> CM HCl = 0,1 b. pH = 4 —> [H+] = 10^-4 —> CM H2SO4 = [H+]/2 = 5.10^-5 mol/l c. pH = 11 —> [H+] = 10^-11 —> [OH-] = 10^-14/[H+] = 10^-3 —> CM KOH = 10^-3 d. pH = 13 —> [H+] = 10^-13 —> [OH-] = 10^-14/[H+] = 0,1 —> CM Ba(OH)2 = [OH-]/2 = 0,05
pH = -log[H+] => [H+] = 10-pH = 10-5M Đáp án cần chọn là: D CÂU HỎI HOT CÙNG CHỦ ĐỀ
Một mẫu nước có pH = 3,82 thì nồng độ mol /l của ion H+ trong đó là Tính pH của 300ml dung dịch (gồm 100 ml Ba(OH)2 0,1M và 200 ml NaOH 0,05M) Dung dịch bazo mạnh Ba(OH)2 có [Ba2+] = 5.10-4. pH của dung dịch này là: Dung dịch HCl 0,1M có pH là:
Một dung dịch có pH = 9,0. Tính nồng độ mol của H+ và OH- trong dung dịch? Hãy cho biết màu của phenolphtalein trong dung dịch này?
Trong một dung dịch C H 3 C O O H , người ta xác định được nồng độ H+ bằng 3. 10 - 3 M và nồng độ C H 3 C O O H bằng 3,97. 10 - 1 M. Tính nồng độ mol ban đầu của C H 3 C O O H .
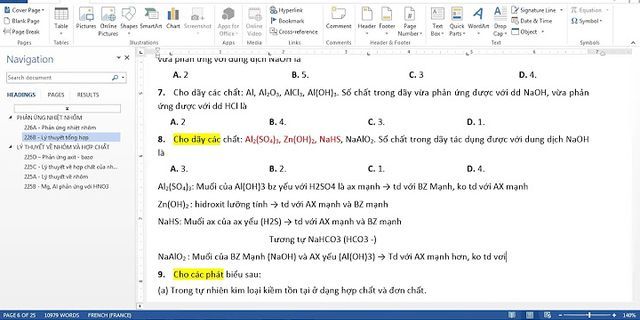
Cho 4 dung dịch loãng, có cùng nồng độ mol: C 2 H 5 COOH , HCl , NH 3 , Ba ( OH ) 2 . Dung dịch có pH nhỏ nhất và lớn nhất lần lượt là A. HCl và NH 3 . B. CH 3 COOH và Ba ( OH ) 2 . C. HCl và Ba ( OH ) 2 D. CH 3 COOH và NH 3 Một dung dịch có pH =5. Tính nồng độ mol của ion H+ và OH- trong dung dịch . Cho biết màu của phenolphtalein trong dung dịch. |