Lời giải của GV Vungoi.vn nSO2(đktc) = 6,72/22,4 = 0,3 (mol); nS = 5,76/32 = 0,18 (mol) Đặt số mol Fe = a (mol) và M = b (mol) BTNT “Fe”: nFe2(SO4)3 = 1/2 nFe = 0,5a (mol) BTNT “M”: nMSO4 = nM = b (mol) Xét hh X tác dụng với H2SO4 đặc, nóng Hệ phương trình: \(\left\{ \begin{array}{l}BTe:3{n_{Fe}} + 2{n_M} = 2{n_{S{O_2}}} + 6{n_S}\\m\,muoi:{m_{F{e_2}{{(SO4)}_3}}} + {m_{MS{O_4}}} = {m_{\,muoi}}\end{array} \right. \Rightarrow \left\{ \begin{array}{l}3a + 2b = 2.03 + 6.0,18\\400.0,5a + (M + 96)b = 105,6\end{array} \right. \Rightarrow \left\{ \begin{array}{l}3a + 2b = 1,68\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,(1)\\200a + (M + 96)b = 105,6\,\,(2)\end{array} \right.\) Xét hh tác dụng với HCl dư; nH2(đktc) = 16,128/22,4 = 0,72 (mol) TH1: Chỉ có Fe tác dụng, M đứng sau H trong dãy điện hóa học nên không phản ứng BTe ta có: 2nFe = 2nH2 ⟹ nFe = nH2 = 0,72 (mol) ⟹ a = 0,72 (mol) ⟹ thay a vào (1) ⟹ b = -0,24 ⟹ loại TH2: Cả Fe và M cùng tác dụng với dd HCl BT e ta có: 2nFe + 2nM = 2nH2 ⟹ a + b = 0,72 (3) giải hệ (2) và (3) ta được a = 0,24 và b = 0,48 Thay a, b vào (2) ta có: 200.0,24 + (M+96).0,48 = 105,6 ⟹ M = 24 (g/mol) Vậy M là Mg Oxit cao nhất của một nguyên tố R ứng với công thức RO2. Nguyên tố R đó là:
Câu hỏiNhận biết
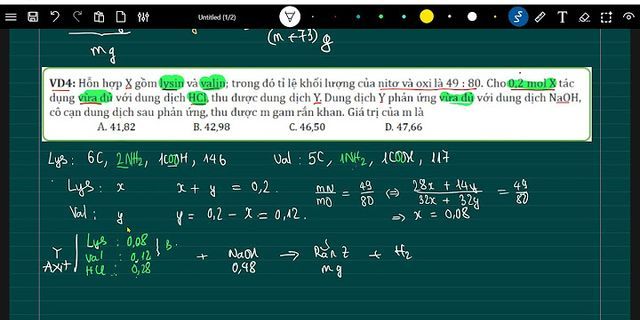
Hòa tan 4,0 gam hỗn hợp Fe và kim loại X có hóa trị II vào dung dịch HCl dư, thu được 2,24 lít khí H2 (đktc). Nếu chỉ dùng 2,4 gam kim loại hóa trị II vào dung dịch HCl thì dùng không hết 500 ml dung dịch HCl 1M. Kim loại hóa trị II đó là:
A. Ca. B. Mg. C. Ba. D. Sr.
Câu hỏi trên thuộc đề trắc nghiệm Đề thi online phương pháp biện luậnLớp 9 Hoá học Lớp 9 - Hoá học
Hòa tan hoàn toàn 0,5 gam Fe và một kim loại hóa trị II trong dung dịch HCl thu được 1,12 lít khí H2 đktc. Kim loại hóa trị II đó là kim loại nào sau đây. A. Mg. B. Ca. C. Zn. D. Be. Các câu hỏi tương tự
Hoà tan hỗn hợp gồm 0,5 gam Fe và một kim loại hoá trị II trong dung dịch HCl dư thu được 1,12 lít khí H2 (đktc). Kim loại hoá trị II đó là: A. Mg B. Ca C. Zn D. Be.
Cho 0,5 gam một kim loại hóa trị II phản ứng hoàn toàn với dung dịch HCl dư, thu được 0,28 lít khí H2 (đktc). Kim loại đó là: A. Mg B. Sr C. Ca D. Ba
Hòa tan hoàn toàn 21 gam hỗn hợp 2 muối cacbonat của kim loại hóa trị I và kim loại hóa trị II bằng dung dịch HCl dư, thu được dung dịch A và 1,008 lít khí (đktc). Cô cạn dung dịch A thì thu được m gam muối khan. Giá trị của m là: A. 24,495 B. 13,898 C. 21,495 D. 18,975
Hòa tan hoàn toàn 21 gam hỗn hợp 2 muối cacbonat của kim loại hóa trị I và kim loại hóa trị II bằng dung dịch HCl dư, thu được dung dịch A và 1,008 lít khí (đktc). Cô cạn dung dịch A thì thu được m gam muối khan. Giá trị của m là: A. 24,495 B. 13,898 C. 21,495 D. 18,975
Hòa tan hoàn toàn 8,45 gam một kim loại hóa trị II bằng dung dịch HCl. Cô cạn dung dịch sau phản ứng thu được 17,68 gam muối khan. Kim loại trên là kim loại nào sau đây? A. Fe B. Mg C. Zn D. Ba
Hòa tan hoàn toàn 8,45 gam một kim loại hóa trị II bằng dung dịch HCl. Cô cạn dung dịch sau phản ứng được 17,68 gam muối khan. Kim loại trên là kim loại nào sau đây? A. Fe. B. Mg. C. Zn. D. Ba.
Hòa tan hoàn toàn 1,1 gam hỗn hợp gồm một kim loại kiềm X và một kim loại kiềm thổ Y ( M X < M Y ) trong dung dịch HCl dư, thu được 1,12 lít khí H2 (đktc). Kim loại X là A. K B. Na C. Rb D. Li
Hòa tan hoàn toàn 14,4 gam kim loại M hóa trị II trong dung dịch HNO3 đặc, dư thu được 26,88 lít NO2 (đktc) là sản phẩm khử duy nhất. Kim loại M là A. Zn B. Cu C. Fe D. Mg
Hòa tan hoàn toàn 24 gam hỗn hợp X gồm MO, M(OH)2 và MCO3 (M là kim loại có hóa trị không đổi) trong 100 gam dung dịch H2SO4 39,2% thu được 1,12 lít khí (đktc) và dung dịch Y chỉ chứa một chất tan duy nhất có nồng độ 39,41%. Kim loại M là A. Cu B. Mg C. Ca D. Zn |